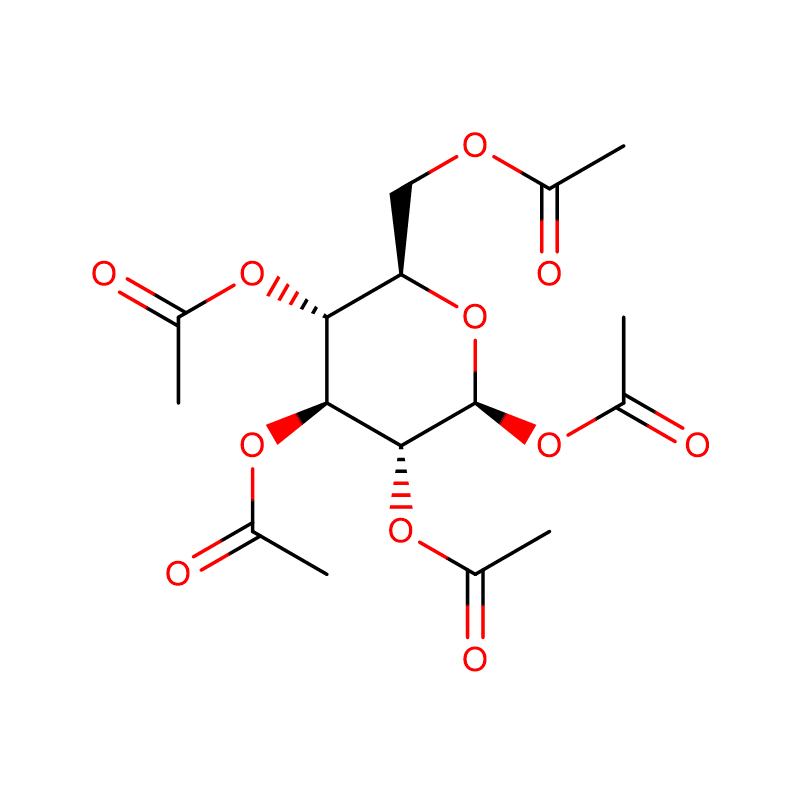
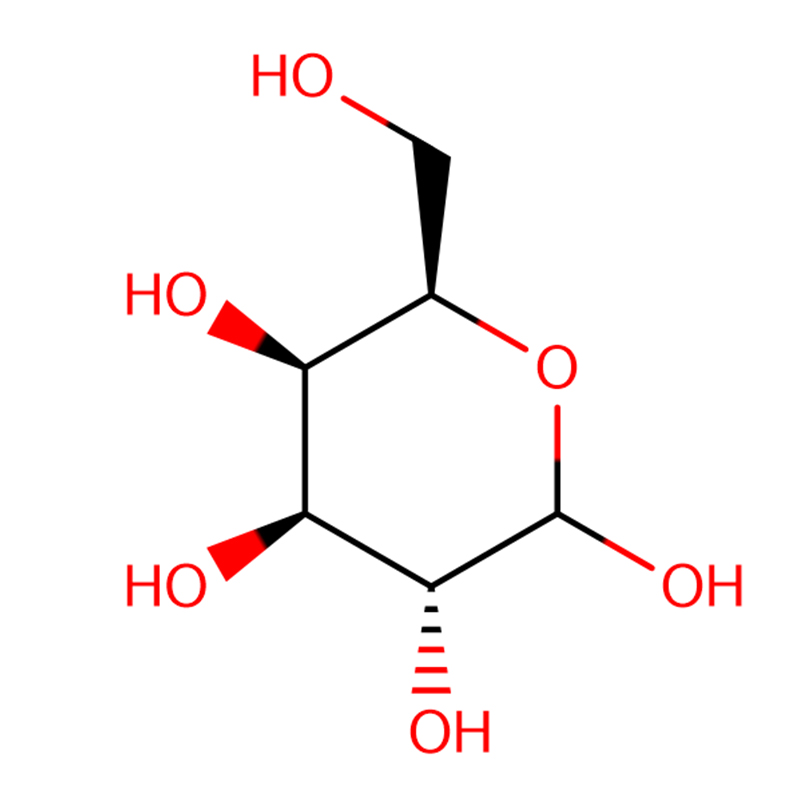
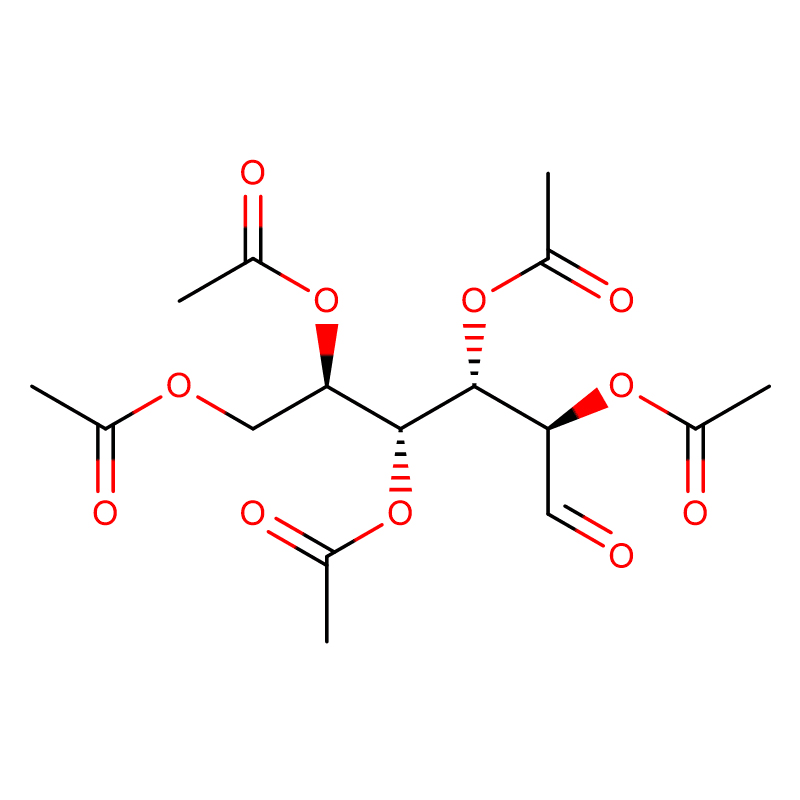
4-NITROPHENYL-ALPHA-D-MANNOPYRANOSIDE CAS: 10357-27-4 gebroken wit poeder 98%
| Catalogus nummer | XD90011 |
| productnaam | 4-nitrofenyl-alfa-D-mannopyranoside |
| CAS | 10357-27-4 |
| Moleculaire formule | C12H15NO8 |
| Molecuulgewicht | 30301.25 |
| Opslaggegevens | -2naar -8° C |
| Geharmoniseerde Tarievencode | 29400000 |
Productspecificatie
| Water | <5% Karl Fische |
| Oplosbaarheid | 1% in DMF is helder en kleurloos |
| Puurheid | Vrij 4-nitrofenol <200ppm |
| HPLC | >98% |
| Verschijning | Gebroken wit poeder |
Mechanistische inzichten in een Ca2+-afhankelijke familie van alfa-mannosidasen in een menselijke darmsymbiont.
Darmbacteriën, geïllustreerd door Bacteroides thetaiotaomicron, spelen een sleutelrol bij het handhaven van de menselijke gezondheid door gebruik te maken van grote families van glycosidehydrolasen (GH's) om voedingspolysacchariden en gastheerglycanen als voedingsstoffen te exploiteren.Een dergelijke uitbreiding van de GH-familie wordt geïllustreerd door de 23 familie GH92-glycosidasen die worden gecodeerd door het B. thetaiotaomicron-genoom.Hier laten we zien dat dit alfa-mannosidasen zijn die werken via een enkel verplaatsingsmechanisme om gastheer-N-glycanen te gebruiken.De driedimensionale structuur van twee GH92-mannosidasen definieert een familie van eiwitten met twee domeinen waarin het katalytische centrum zich op de domeininterface bevindt, die zuur (glutamaat) en base (aspartaat) helpen bij hydrolyse in een Ca(2+)- afhankelijke manier.De driedimensionale structuren van de GH92's in combinatie met remmers geven inzicht in de specificiteit, het mechanisme en de conformatieroute van katalyse.Ca(2+) speelt een belangrijke katalytische rol bij het helpen vervormen van het mannoside weg van zijn conformatie in de grondtoestand (4)C(1)-stoel naar de overgangstoestand. (Bibliografie: Nat.Chem.Biol.6, 125-32, (2010)
Frontale affiniteitschromatografie van ovalbumineglycoasparagines op een concanavaline A-Sepharose-kolom.Een kwantitatieve studie van de bindingsspecificiteit van het lectine.
De interacties van Sepharose 4B-geïmmobiliseerd concanavaline A (ConA) met 10 glycoasparagines afgeleid van ovalbumine werden kwantitatief onderzocht door middel van frontale affiniteitschromatografie.Bij deze methode wordt continu een koolhydraatoplossing op een ConA-Sepharose-kolom aangebracht en wordt de vertraging van het elutiefront gemeten als een parameter van de sterkte van de interactie.De dissociatieconstante (Kd) voor elke saccharide met ConA kan worden bepaald.Een analyse van de binding van p-nitrofenyl-alfa,D-mannoside heeft aangetoond dat de bindingseigenschappen van ConA niet wezenlijk veranderen na immobilisatie op Sepharose 4B.Elk van de ovalbumineglycoasparagines werd gelabeld met tritium door de reductieve methyleringsmethode voor analyse.Een vergelijking van de verkregen Kd-waarden toonde aan dat de binding van ConA aanzienlijk varieert met zeer kleine structurele verschillen van de glycosylketen.De resultaten suggereren dat ConA een specifieke glycosylketenstructuur herkent, Man alfa 1-6 (Man alfa 1-3) Man, waarin ten minste één hydroxylgroep op de C-3-positie van C-6-gekoppelde mannose vrij zou moeten zijn.