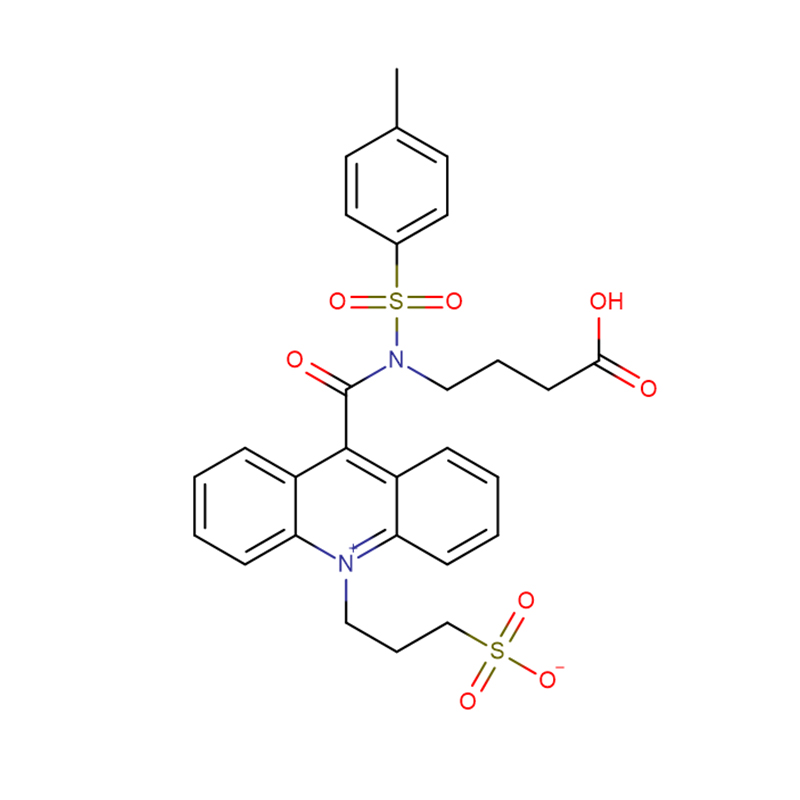
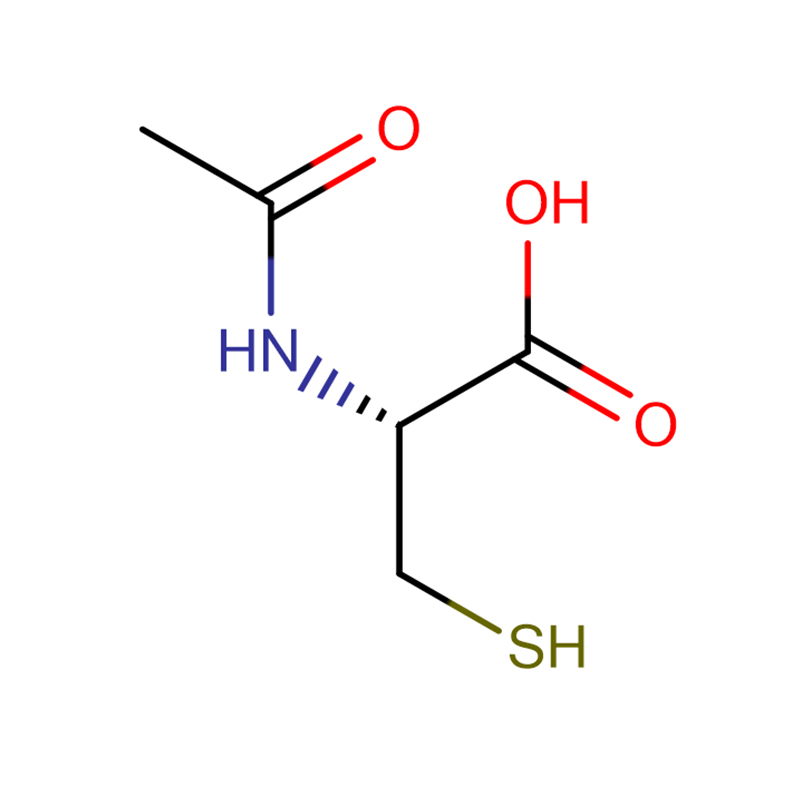
4-Amino-3-hydrazino-1,2,4-triazool-5-thiol Cas:28836-03-5 99% gele tot groene vaste stof
| Catalogus nummer | XD90146 |
| productnaam | 4-Amino-3-hydrazino-1,2,4-triazool-5-thiol |
| CAS | 28836-03-5 |
| Moleculaire formule | C16H13NO3S·NH3 |
| Molecuulgewicht | 316.37 |
| Opslaggegevens | Omgeving |
| Geharmoniseerde Tarievencode | 2923900090 |
Productspecificatie
| Verschijning | Geel tot groen vast |
| Assay | ≥ 99% |
| Smeltpunt | 237°C(dec.)(lit.) |
| Oplosbaarheid | NaOH: oplosbaar1 N |
| In water oplosbaar | Oplosbaar in water, 1N NaOH en methanol. |
1. We bestudeerden de remmende effecten van isorhamnetin op paddestoeltyrosinase door remmingskinetiek en computationele simulatie.Isorhamnetin remde reversibel tyrosinase op een gemengde manier bij Ki=0,235 ± 0,013 mM.Metingen van intrinsieke en 1-anilinonaftaleen-8-sulfonaat (ANS)-bindende fluorescentie toonden aan dat isorhamnetine geen significante veranderingen in de tertiaire structuur van tyrosinase veroorzaakte.Om inzicht te krijgen in het inactivatieproces, werd de kinetiek berekend via tijdsintervalmetingen en continue substraatreacties.De resultaten gaven aan dat inactivatie geïnduceerd door isorhamnetin een reactie van de eerste orde was met bifasische processen.Om meer inzicht te krijgen, simuleerden we koppeling tussen tyrosinase en isorhamnetin.Simulatie was succesvol (bindingsenergieën voor Dock6.3: -32,58 kcal/mol, voor AutoDock4.2: -5,66 kcal/mol, en voor Fred2.2: -48,86 kcal/mol), wat suggereert dat isorhamnetine interageert met verschillende residuen, zoals als HIS244 en MET280.Deze strategie van het voorspellen van tyrosinase-interactie in combinatie met kinetiek op basis van een flavanonverbinding zou nuttig kunnen zijn bij het screenen op potentiële natuurlijke tyrosinaseremmers.
2.Zuurontvouwingsroute van conalbumine (CA), een monomeer glycoproteïne uit kippenei-eiwit, is onderzocht met behulp van ver- en nabij-UV CD-spectroscopie, intrinsieke fluorescentie-emissie, extrinsieke fluorescentiesonde 1-anilino-8-naftaleensulfonaat (ANS) en dynamische lichtverstrooiing (DLS).We observeren pH-afhankelijke veranderingen in de secundaire en tertiaire structuur van CA.Het heeft native-achtige α-helix secundaire structuur bij pH 4,0 maar verliesstructuur bij pH 3,0.De CA bestond uitsluitend als een pre-gesmolten bolletjestoestand en gesmolten bolletjestoestand in oplossing bij respectievelijk pH 4,0 en pH 3,0.Het effect van pH op de conformatie en thermostabiliteit van CA wijst op zijn hittebestendigheid bij neutrale pH.DLS-resultaten laten zien dat de MG-toestand bestond als compacte vorm in waterige oplossingen met hydrodynamische stralen van 4,7 nm.Het doven van de fluorescentie van tryptofaan door acrylamide bevestigde verder de accumulatie van een tussentoestand, gedeeltelijk ongevouwen, tussen natuurlijke en ongevouwen toestanden.


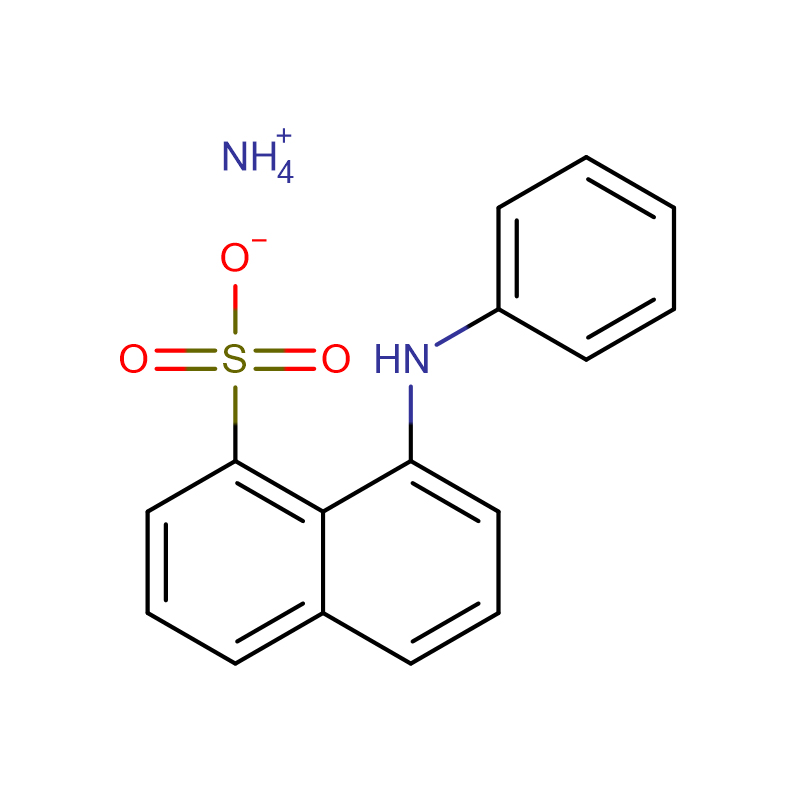


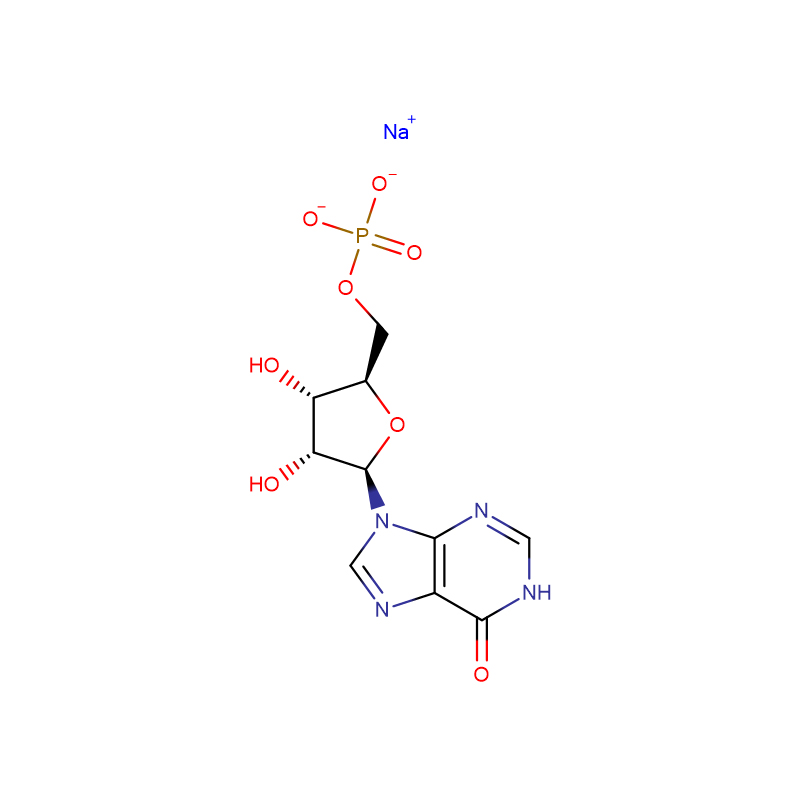
![N-[[bis[4-(dimethylamino)fenyl]amino]carbonyl]glycine natriumzout Wit tot grijsgroen kristallijn poeder](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)